
Científicos del Cibir desarrollan una novedosa vacuna contra tumores sólidos como los de mama y colon
La unidad de angiogénesis logra con su tratamiento de ARN mensajero disminuir el número y tamaño de las metástasis
Adriana Iruzubieta
Logroño
Viernes, 18 de julio 2025, 13:34
Avances científicos esperanzadores para los enfermos de cáncer llegan de la mano de la unidad de angiogénesis del Cibir, que ha desarrollado una vacuna terapéutica, no preventiva, de ARN mensajero para frenar tumores sólidos y metástasis.
Las grandes compañías farmacéuticas, Pfizer, Moderna, Merck; ya están desarrollando estos tratamientos con ARN y algunos ya se encuentran en la tercera fase, con lo cual en un par de años ya estarán disponibles en la clínica. El doctor Alfredo Martínez, jefe de la unidad, ha augurado grandes avances en este ámbito «en melanoma metastásico estas vacunas producen un aumento del 50 por ciento de la supervivencia de los pacientes». La unidad ha logrado que por primera vez se haga frente a una diana de angiogénesis (dirigida contra la adrenomedulina) y que, como asegura el doctor, «funciona». Esta innovación sería útil para tumores sólidos, todos los que son distintos de los referidos a la sangre.
Esto representa un avance en terapias personalizadas contra el cáncer. , Son tratamientos primordiales para adecuar la cura al tipo de tumor específico de cada persona en el momento que se va a implementar la vacuna. Con este avance se produce una respuesta inmunitaria dirigida hasta a 35 dianas terapéuticas. Cada cáncer es diferente y por ello necesita una terapia particular.
La angiogénesis, ha explicado el doctor Martínez, «es la formación de nuevos vasos sanguíneos» que en el contexto del cáncer cuando el tumor va necesitando más oxígeno y nutrición lanza señales para producir más. Con esta terapia quieren «parar este proceso y que no crezca». Este procedimiento ya han podido demostrarlo en ratones con tumores de melanoma que producen metástasis al pulmón, una vez que los vacunan desarrollan anticuerpos frente a esa proteína sintetizada. Los vasos sanguíneos externos al tejido canceroso no resultan afectados lo que se traduce en la pérdida de efectos secundarios en el paciente.

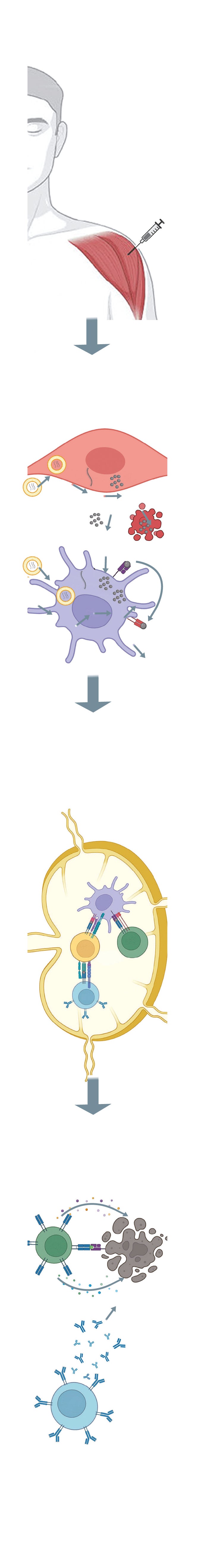
Mecanismo de acción
de las vacunas de ARNm
contra el cáncer
A
Administración
intramuscular de la
vacuna empaquetada
en la nanopartícula
B
El ARNm entra en la célula
muscular y produce la
proteína diana
Célula
muscular
Tumor
antígeno
ARNm
ARNm
encapsulado
Antígenos
tumorales
MHCI
ARNm
MHCI
C
Las células presentadoras de
antígenos (APC) captan la nueva
proteína y migran a los ganglios
linfáticos locales o al bazo
APC
CD8+
CD4+
Nodo
linfático
Célula
B
D
Las APC presentan los antígenos
tumorales a los linfocitos T CD4+
y CD8+, y de ese modo los activan
PFN
GzmB
CTL
IFNy
TNFa
Célula
cancerosa
muerta
Célula
plasmática
E
Los linfocitos activados migran
desde los ganglios linfáticos al
tumor donde, tras reconocer a
las células diana, son capaces
de inducir la destrucción de las
células tumorales.
Mecanismo de acción
de las vacunas de ARNm
contra el cáncer
A
Administración
intramuscular de la
vacuna empaquetada
en la nanopartícula
B
El ARNm entra en la célula
muscular y produce la
proteína diana
Célula
muscular
Tumor
antígeno
ARNm
ARNm
encapsulado
Antígenos
tumorales
MHCI
ARNm
MHCI
C
Las células presentadoras de
antígenos (APC) captan la nueva
proteína y migran a los ganglios
linfáticos locales o al bazo
APC
CD8+
CD4+
Nodo
linfático
Célula
B
D
Las APC presentan los antígenos
tumorales a los linfocitos T CD4+
y CD8+, y de ese modo los activan
PFN
GzmB
CTL
IFNy
TNFa
Célula
cancerosa
muerta
Célula
plasmática
E
Los linfocitos activados migran
desde los ganglios linfáticos al
tumor donde, tras reconocer a
las células diana, son capaces
de inducir la destrucción de las
células tumorales.
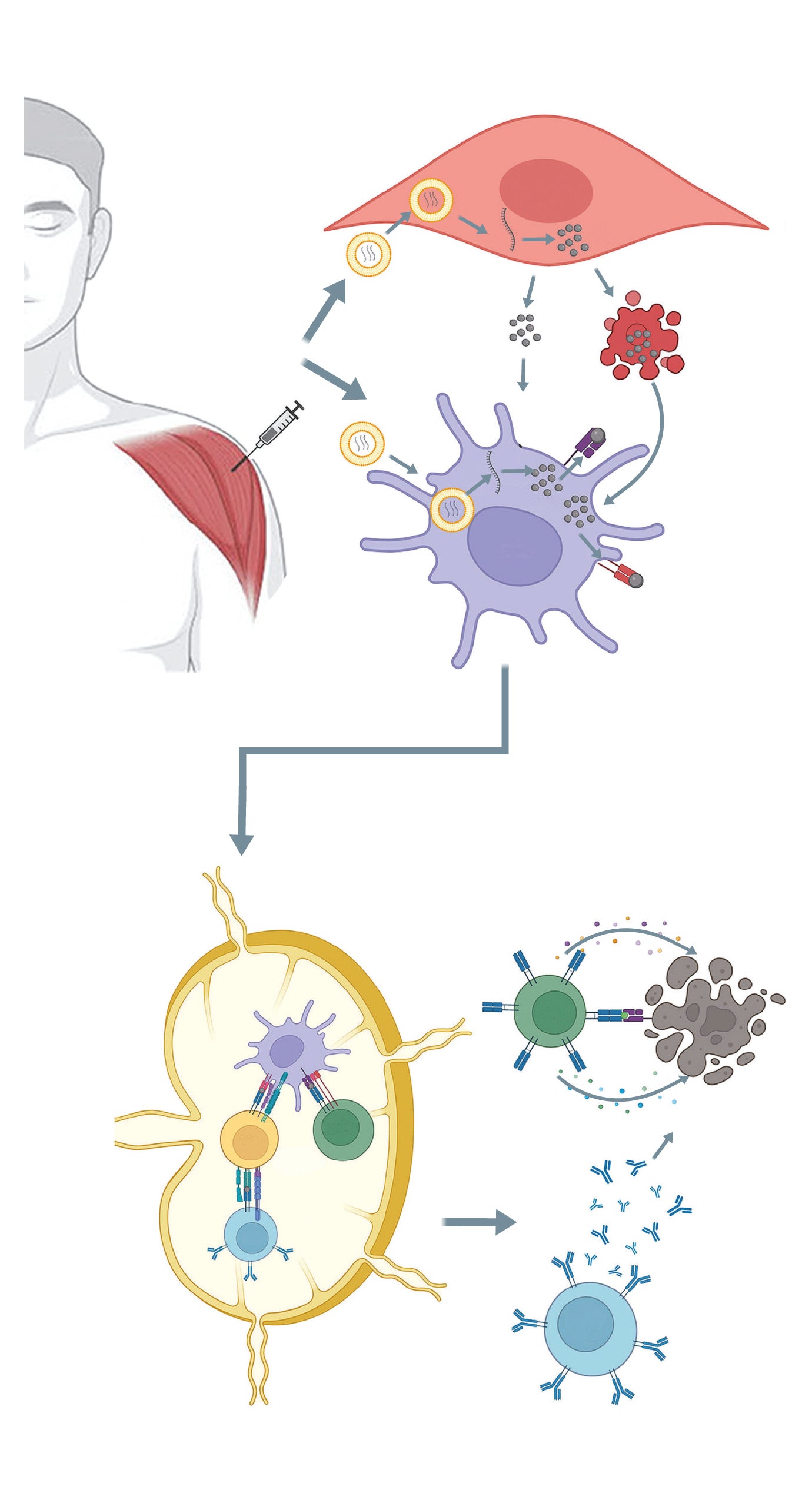
Mecanismo de acción de las vacunas
de ARNm contra el cáncer
Célula
muscular
Tumor
antígeno
A
ARNm
Administración
intramuscular de la
vacuna empaquetada
en la nanopartícula
ARNm
encapsulado
Antígenos
tumorales
Célula
moribunda
con
antígenos
tumorales
MHCI
ARNm
APC
B
MHCI
El ARNm entra
en la célula
muscular
y produce la
proteína diana
D
Las APC presentan los antígenos tumorales
a los linfocitos T CD4+ y CD8+, y
de ese modo los activan
C
Las células
presentadoras de
antígenos (APC)
captan la nueva
proteína y
migran a los
ganglios
linfáticos
locales o
al bazo
PFN
GzmB
CTL
APC
IFNy
TNFa
Célula
cancerosa
muerta
CD8+
CD4+
Nodo
linfático
Célula
B
Célula
plasmática
E
Los linfocitos activados migran desde los ganglios linfáticos
al tumor donde, tras reconocer a las células diana, son capaces
de inducir la destrucción de las células tumorales.
Al igual que la vacuna del covid, es una inyección de una molécula de ARN sintético que se introduce en una nanopartícula lipídica -que transporta medicamentos o sustancias por el cuerpo de manera controlada y eficiente- y el organismo de la persona enferma producirá anticuerpos frente a la proteína que se sintetiza.
La adrenomedulina es la molécula clave en la angiogénesis tumoral hacia la que se ha dirigido la aportación del Cibir. Es una proteína que actúa como regulador en ese proceso y está sobreexpresada en la mayoría de tumores sólidos, por ello es la partícula ideal para la inmunoterapia. El organismo humano produce la adrenomedulina naturalmente y para conseguir que el cuerpo humano produjese anticuerpos tuvieron que unirla a una proteína de un caracol marino para conseguir el efecto deseado.



